Messung der Biomolekülkonzentration in GMP- und Non-GMP-Tests
Konzentrationsmessung von Biomolekülen
Aufgrund ihrer Spezifität, zerstörungsfreien Natur und schnellen Messgeschwindigkeit ist die Multiwellenlängen-UV/DUV-Spektroskopie die bevorzugte Technik zur Messung der Biomolekülkonzentration (Singh et al. 2021; Carvalho et al. 2025). Biomoleküle wie Proteine, Peptide, monoklonale Antikörper, mRNA/DNA und Aminosäuren absorbieren Licht bei spezifischen UV/DUV-Wellenlängen.
Proteine absorbieren überwiegend bei 280 nm und unter 220 nm aufgrund der aromatischen Seitenketten von Tryptophan, Tyrosin und Phenylalanin (Antosiewicz und Shugar 2016). Das Verhältnis der Wellenlängen in diesem Bereich kann verwendet werden, um das Protein für Fraktionierung, Identifikation, Qualitätskontrolle und realtime release Anwedungen zu erfassen (Carvalho et al. 2025; Farag et al. 2022; Schmid (2008); He et al. 2019).
RNA absorbiert überwiegend bei 260 nm, was die Grundlage für die Quantifizierung ihrer Konzentration und die Bewertung der Reinheit aufgrund der konjugierten Doppelbindungen in ihren Nukleotidbasen bildet. Das Verhältnis von Absorption bei 260 nm zur Absorption bei 280 nm (A260/A280) hilft, die RNA-Reinheit zu bestimmen; ein Verhältnis von etwa 2,0–2,1 weist auf hohe Reinheit hin, während niedrigere Werte auf eine Proteinkontamination hindeuten können (Wilfinger et al. 1997; Imbeaud 2005; Gomes 2021).
Aufgrund der Vielfalt an Hilfsstoffen sind bislang mehrere Offline-Methoden erforderlich. Herkömmliche Online-Methoden wie Raman oder FT-NIR erfordern Modellbildung, Pflege und Überwachung. Sie überzeugen in der Praxis oft nur bedingt.
Die Überwachung von sehr hohen Proteinkonzentrationen in der Biotechnologie
Die genaue Quantifizierung von DNA- oder Proteinwerten in Zellextrakten ist ein Grundpfeiler der modernen Bioprozessierung. Während die Branche auf ausgefeilte monoklonale Antikörpertherapien (mAb) und verbesserte Produktionstechnologien umsteigt, war die Nachfrage nach Echtzeit-Online-Überwachung nie größer. Dieser Wandel hat neue Methoden zur Messung außergewöhnlich hoher Proteinkonzentrationen erforderlich gemacht, oft zwischen 40 und 500 mg/mL und manchmal sogar noch höher.
In einem typischen Chromatographie-Setup sind 215 nm und 280 nm UV-Sensoren der Goldstandard zur Erkennung von Kleinstmengen von Proteinen mit hoher Präzision, was diese Wellenlängen ideal macht, um Fraktions-Sammelfenster zu bestimmen. Bei den sehr hohen Konzentrationen, die in der fortgeschrittenen Biofertigung erforderlich sind, wird das Instrument selbst bei deutlich verkürzter optischer Pfadlänge bei diesen Wellenlängen oft vom Maßstab abfallen.
Um sehr hohe Konzentrationen genau zu messen, ist die einfachste Lösung die Verwendung einer zweiten Wellenlänge. Dieser Ansatz stellt sicher, dass das Photometer in seinem idealen linearen Bereich arbeitet und während des gesamten Elutionsprozesses zuverlässige Daten liefert.
Vorteile der Multi-Wellenlängen-Technologie
Mehrwellenlängenspektroskopie wurde eingeführt, um Einschränkungen bei höheren Konzentrationen aufgrund der Signalsättigung und der Nichtlinearität des Beer-Lambert-Gesetzes zu überwinden (Chen, Z et al. 2018, Vanderlinde 1982).
Das Kemtrak SPECTRA ist ein industrielles Prozessphotometer, das ein Diodenarray-
Spektrophotometer mit fester optischer Weglänge verwendet und durch Einfachheit und
Zuverlässigkeit eine überlegene Alternative bietet:
- Sofortige Messung: Ohne bewegliche Teile erfolgt die Datenerhebung in Echtzeit und kontinuierlich
- In-Line Validierung: Der Analysator kann in-situ mit NIST-nachverfolgbaren Standards validiert werden, ohne das Produkt aus der Prozesslinie zu entfernen.
- Betriebseffizienz: Durch die Beseitigung mechanischer Systemkomponenten minimiert das System den Wartungsbedarf und senkt die total cost of ownership (TCO).
- Unbeeinträchtigte Genauigkeit: Die Messungen werden mit rückverfolgbaren Standards validiert, was das höchste Maß an Vertrauen sowohl in GMP- als auch in Nicht-GMP Umgebungen sicherstellt.
Multiwellenlängenmessung anhand eines Beispiels mit Rinderserum-Albumin
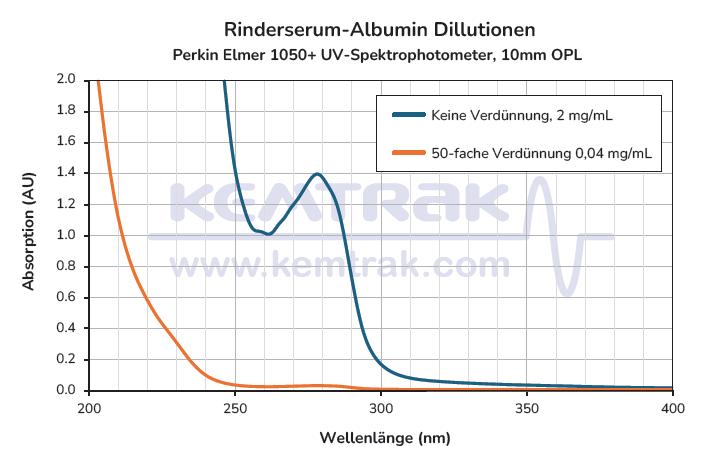
Absorptionsspektrum des Bovine Serum Albumin (BSA) Standard, 2 mg/mL (Thermo Scientific Product Number: 23210, Lot: XA341285) mit einem Perkin Elmer Lambda 1050+ UV/Vis/NIR Laborspektrophotometer. Hohe Konzentrationen (2 mg/mL) können nach einer 50-fachen Verdünnung über 250 nm oder unter 250 nm gemessen werden zur Fraktionierung und unerwünschten Ertragsverlust führen.
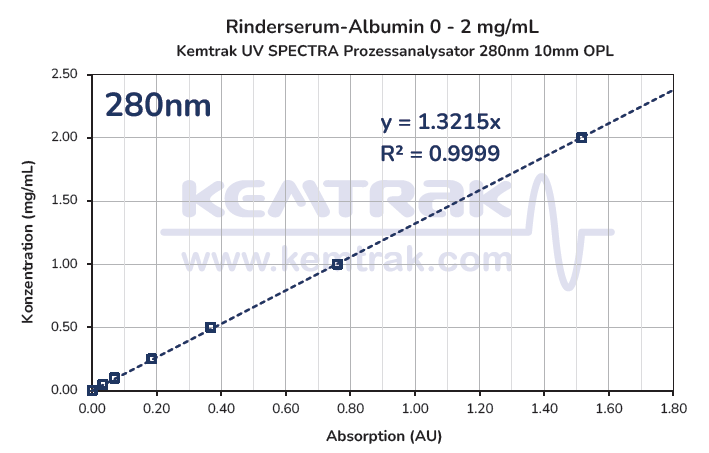
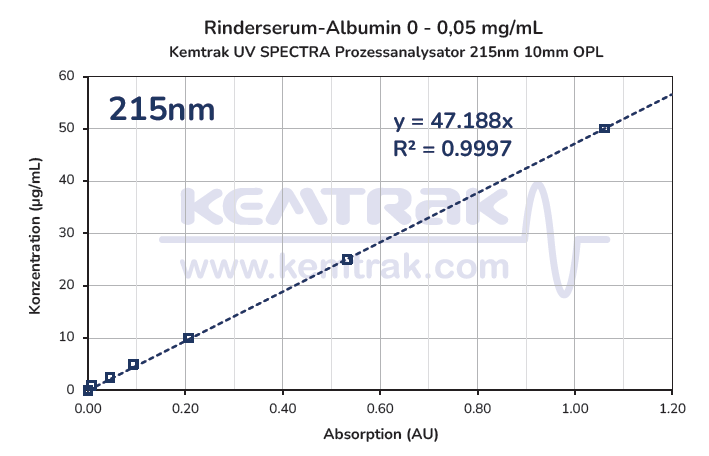
Das Kemtrak SPECTRA ist in der Lage, kontinuierliche Multiwellenlängenmessungen von Bovinem Serumalbumin (BSA) über ein breites Spektrum hinweg durchzuführen, von konzentrierten Werten (2 mg/mL) bis hin zu Spurwerten (0,001 mg/mL). Durch die gleichzeitige Überwachung zweier Wellenlängen, 215 nm und 280 nm, unter Verwendung einer festen optischen Pfadlänge von 10 mm, erhält das System eine hohe Präzision. Bemerkenswert ist, dass der r2-Wert 0,999 übersteigt, was eine lineare Reaktion zwischen Absorption und Konzentration über den gesamten Messbereich zeigt.
Kemtrak SPECTRA (Diodenarray-Spektrophotometer):
Dieses System verwendet ein festes Gitter und ein Array von Photodioden, um das gesamte Spektrum gleichzeitig zu messen. Diese Architektur ermöglicht eine extrem schnelle Datenerfassung und hohe Zuverlässigkeit, da keine beweglichen Teile vorhanden sind. Diodenarray-Systeme können anfällig für höhere Streulichtstufen und eine geringere spektrale Auflösung im Vergleich zu Scanmodellen sein und werden daher typischerweise unter 2,0 AU für maximale Genauigkeit betrieben; sie sind die einzige Wahl für die Echtzeit-Prozessüberwachung, bei der sofortige, mehrwellige Daten erforderlich sind.
Autor des Originalartikel ist Matthew Rice.
Hier finden Sie den gesamten Artikel.
Quellen:
Carvalho et al. (2025): “A review on quantitative process analytical technology for continuous downstream processing of monoclonal antibodies.” Biotechnology and Bioengineering.
Chen et al. (2018): “A mathematical analysis of deviations from linearity of Beer’s law.” Measurement Science and Technology.
Farag et al. (2022): “UV Fingerprinting Approaches for Quality Control Analyses of Food and Functional Food Coupled to Chemometrics.” Foods, 11(18), 2867.
Gomes et al. (2021): “UV-induced fingerprint spectroscopy: A new tool in a toolbox of analytical methods.” Food Chemistry, 368, 130830.
He et al. (2019): “A method to probe protein structure from UV absorbance spectra.” Analytical Biochemistry.
Imbeaud et al. (2005): “Towards standardization of RNA quality assessment using user-independent classifiers of microcapillary electrophoresis traces.” Nucleic Acids Research, 33(6), e56.
Schmid (2008): “Determining the identity and purity of recombinant proteins by UV absorption spectroscopy.” Current Protocols in Protein Science.
Singh et al. (2021): “Multi-wavelength UV-based PAT tool for measuring protein concentration and monitoring protein aggregation in continuous chromatography”. Journal of Chemical Technology & Biotechnology, 96(10), 2824–2834.
Vanderlinde (1982): “Introduction to Multiple-Wavelength Spectrophotometric Analysis.” Clinical Laboratory.
Wilfinger et al. (1997): “Effect of pH and ionic strength on the spectrophotometric assessment of nucleic acid purity.” BioTechniques, 22(3), 474–481.